吸入制剂
来源:四部 分类:通则 页码:130111 吸入制剂 吸入制剂系指原料药物溶解或分散于合适介质中,以蒸气或气溶胶形式递送至肺部发挥局部或全身作用的液体或固体制剂。根据制剂类型,处方中可能含有抛射剂、共溶剂、稀释剂、抑菌剂、助溶剂和稳定剂等,所用辅料应不影响呼吸道黏膜或纤毛的功能。吸入制剂包括吸入气雾剂、吸入粉雾剂、供雾化器用的液体制剂和可转变成蒸气的制剂。
吸入制剂在生产和贮藏中应符合以下规定。
一、吸入制剂的配方中若含有抑菌剂,除另有规定外,在制剂确定处方时,该处方的抑菌效力应符合抑菌效力检查法(通则1121)的规定。吸入液体制剂应为无菌制剂。
二、配制粉雾剂时,为改善粉末的流动性,可加入适宜的载体和润滑剂。吸入粉雾剂中所有附加剂均应为生理可接受物质,且对呼吸道黏膜和纤毛无刺激性、无毒性。
三、吸入制剂中所用给药装置使用的各组成部件均应采用无毒、无刺激性、性质稳定、与原料药物不起作用的材料制备。
四、可被吸入的气溶胶粒子应达一定比例,以保证有足够的剂量可沉积在肺部。吸入制剂中微细粒子剂量应采用相应方法进行表征。
五、吸入制剂中原料药物粒度大小通常应控制在10μm以下,其中大多数应在5μm以下。
六、定量吸入制剂应进行递送剂量均一性检查。多剂量吸入制剂仅测定单个吸入装置内的递送剂量并不足够。生产时应采用合适的方法评价吸入剂罐(瓶)内和罐(瓶)间的递送剂量均一性。
七、吸入气雾剂生产中应进行泄漏检查。
八、定量吸入制剂说明书应标明:①总揿(吸)次;②每揿(吸)主药含量;③临床最小推荐剂量的揿(吸)次;④如有抑菌剂,应标明名称。
九、胶囊型、泡囊型吸入粉雾剂说明书应标明:①每粒胶囊或泡囊中药物含量;②胶囊应置于吸入装置中吸入,而非吞服;③有效期;④贮藏条件。
1.吸入气雾剂
吸入气雾剂系指含药溶液、混悬液或乳液,与合适抛射剂或液化混合抛射剂共同装封于具有定量阀门系统和一定压力的耐压容器中,使用时借助抛射剂的压力,将内容物呈雾状物喷出,用于肺部吸入的制剂。可添加共溶剂、增溶剂和稳定剂。
除另有规定外,吸入气雾剂应进行以下相应检查。
【递送剂量均一性】吸入气雾剂照下述方法测定,应符合规定。
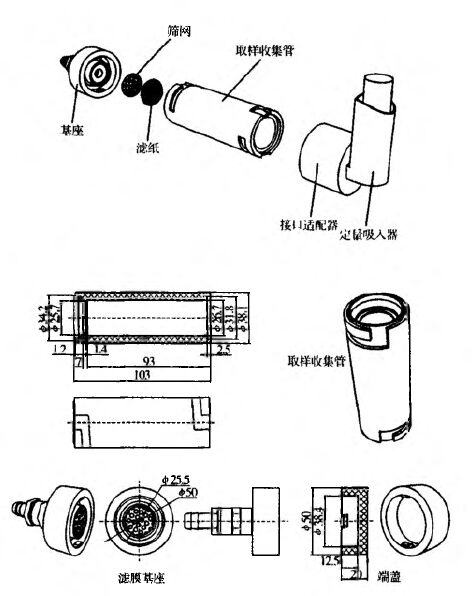
测定装置 包括一个带有不锈钢筛网、用以放置滤纸的基座,一个配有两个密封端盖的取样收集管和一个吸嘴适配器,以确保取样收集管与吸嘴间的密封性(图1)。该装置能定量收集吸入气雾剂的递送剂量。
采用合适的适配器确保气雾剂吸嘴端口与样品收集管口或2.5mm的缩肩平齐。在基座内放入直径为25mm的圆形
图1 吸入气雾剂的递送剂量均一性测定装置(单位:mm)
滤纸,固定于取样收集管的一端。基座端口连接真空泵、流量计。连接测定装置和待测气雾剂,调节真空泵使其能够以28.3L/min流速从整套装置抽气,包括滤纸和待测气雾剂。 空气应持续性从装置抽出,避免活性物质损失进入空气。组装后装置各部件之间的连接应具有气密性,从取样收集管中抽出的所有空气经过待测吸入剂。
测定法 取供试品1罐(瓶),振摇5秒,弃去1喷,将吸入装置插入适配器内,喷射1次,抽气5秒,取下吸入装置。重复上述过程收集产品说明书中的临床最小推荐剂量。用适当溶剂清洗滤纸和收集管内部,合并清洗液并稀释至一定体积。
分别测定标示揿次前(初始3个剂量)、中(n/2吸起4个剂量,n为标示总揿次)、后(最后3个剂量),共10个递送剂量。
采用各品种项下规定的分析方法,测定各溶液中的药量。
对于含多个活性成分的吸入剂,各活性成分均应进行递送剂量均一性检测。
结果判定 符合下述条件之一者,可判为符合规定。
(1)10个测定结果中,若至少9个测定值在平均值的75%~125%之间,且全部在平均值的65%~135%之间。
(2)10个测定结果中,若2~3个测定值超出75%~125%,另取2罐(瓶)供试品测定。若30个测定结果中,超出75%~125%的测定值不多于3个,且全部在平均值的65%~135%之间。
吸入气雾剂产品放行时需作罐(瓶)间递送剂量均一性测定。取10罐(瓶)供试品,采用上述收集管分别收集1个产品说明书中的临床最小推荐剂量,共10个递送剂量。
结果判定 符合下述条件者,可判为符合规定。
(1)10个测定结果中,若不少于9个测定值在平均值的75%~125%之间,且全部在平均值的65%~135%之间。
(2)10个测定结果中,若2~3个测定值超出75%~125%,但全部在平均值的65%~135%之间,另取20罐(瓶)供试品测定。若30个剂量中,超出75%~125%的测定值不多于3个,且全部在平均值的65%~135%之间。
【每瓶总揿次】照下述方法检查,应符合规定。
检查法 取气雾剂1罐(瓶),揿压阀门,释放内容物到废弃池中,每次揿压间隔不少于5秒。每罐(瓶)总揿次应不少于标示总揿次(此检查可与递送剂量均一性测试结合)。
【微细粒子剂量】照吸入制剂微细粒子空气动力学特性测定法(通则0951)检查,照各品种项下规定的装置与方法,依法测定,计算微细粒子剂量,应符合各品种项下规定。除另有规定外,微细药物粒子百分比应不少于每吸主药含量标示量的15%。
呼吸驱动的吸入气雾剂应对以上检查项的操作按各品种使用说明书进行相应调整。
【微生物限度】除另有规定外,照非无菌产品微生物限度检查:微生物计数法(通则1105)和控制菌检查法(通则1106)及非无菌药品微生物限度标准(通则1107)检查,应符合规定。
2.吸入粉雾剂
吸入粉雾剂系指固体微粉化原料药物单独或与合适载体混合后,以胶囊、泡囊或多剂量贮库形式,采用特制的干粉吸入装置,由患者吸入雾化药物至肺部的制剂。
除另有规定,吸入粉雾剂应进行以下检查。
【递送剂量均一性】吸入粉雾剂照下述方法测定,应符合规定。
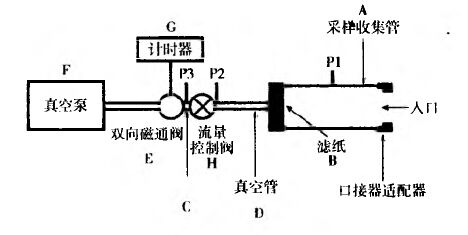
测定装置 与吸入气雾剂递送剂量均一性测定装置类似,但取样收集管和滤纸的尺寸需与测定流速相匹配,装置及参数如图2及附表1。
装置入口端安装合适的适配器,确保吸入剂吸嘴端口与样品收集管口平齐。在基座内放入圆形滤纸,固定于取样收集管的一端。基座端口与真空泵相连,连接装置。取吸入装置,插入适配器。开启真空泵,打开双向磁通阀,调节流量控制阀使吸入装置前后的压力差(P1)为4.0kPa。取下吸入装置,在装置入口连接流量计,测定离开流量计的体积流量Qout。对于测定进入体积流量Qin的流量计,可按下式换算:
Qout=(Qin×PO)/(PO-ΔP)
PO):大气压
式中 ΔP为流量计前后压差。
图2 吸入粉雾剂递送剂量均一性测定装置
若流速大于l00L/min,调节流量至100L/min,若流速小于l00L/min,保持流速不变,流速记为Qout。计算抽气时间T=(4×60)/Qout,单位为秒。记录P2及P3值,P3/P2应不大于0.5。
根据产品说明书准备供试品,将供试品插入适配器内,开启真空泵,抽吸T秒。关闭真空泵,取下吸入装置。重复上述过程收集产品说明书中的临床最小推荐剂量。以空白溶剂清洗滤纸和收集管内部,合并清洗液并稀释至一定体积。
胶囊或泡囊型粉雾剂重复上述过程测定10个剂暈。贮库型粉雾剂分别测定标示揿次前(初始3个剂量)、中(n/2吸起4个剂量,n为标示总揿次)、后(最后3个剂量),共10个递送剂量。
采用各品种项下规定的分析方法,测定各溶液中的药量。
对于含多个活性成分的吸入剂,各活性成分均应进行递送剂量均一性检测。
结果判定 同“吸入气雾剂”项下要求。
贮库型吸入粉雾剂罐(瓶)间递送剂量均一性测定同“吸入气雾剂”项下方法。
【微细粒子剂量】照吸入制剂微细粒子空气动力学特性测定法(通则0951)检查,照各品种项下规定的装置与方法,依法测定,计算微细粒子剂量,应符合规定。除另有规定外,微细药物粒子百分比应不少于每吸主药含量标示量的10%。
【多剂量吸入粉雾剂总吸次】在设定的气流下,将吸入剂揿空,记录揿次,不得低于标示的总揿次(该检查可与递送剂量均一性测定结合)。
【微生物限度】除另有规定外,照非无菌产品微生物限度检查:微生物计数法(通则1105)和控制菌检查法(通则1106)及非无菌药品微生物限度标准(通则1107)检查,应符合规定。
3.供雾化器用的液体制剂
供雾化器用的液体制剂系指通过连续或定量雾化器产生供吸入用气溶胶的溶液、混悬液和乳液。
连续型和定量雾化器均是一类通过高压气体、超声震动或其他方法将液体转化为气溶胶的装置。前者为吸入液体制剂,可使被吸入的剂量以一定速率和合适的粒径大小沉积在肺部;后者即为定量吸入喷雾剂,可使一定量的雾化液体以气溶胶的形式在一次呼吸状态下被吸入。
用于连续型雾化器的浓缩液使用前采用规定溶液稀释至处方量体积。雾化液体也可由粉末制得。用于连续型雾化器的吸入液体,使用前其pH值应在3~8.5范围内;混悬液和乳液振摇后应具备良好的分散性,可保证递送剂量的准确性;除非制剂本身具有足够的抗菌活性,多剂量水性雾化溶液中可加入合适浓度的抑菌剂,除另有规定外,在制剂确定处方时,该处方的抑菌效力应符合抑菌效力检查法(通则1121)的规定。
除另有规定外,供雾化器用的液体制剂应进行以下检查。
【递送速率和递送总量】吸入液体制剂照下述方法测定,应符合规定。
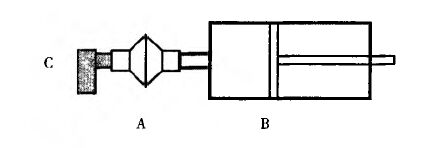
测定装置 由呼吸模拟器和过滤系统组成。呼吸模拟器需能够模拟不同呼吸特性(附表2),过滤系统为经验证的低阻滤纸,能够定量收集气溶胶,并通过适宜溶剂回收活性物质。滤纸罩死体积应不超过呼吸模拟器潮气量的10%。
图3 吸入液体制剂递送速率和递送总量测定装置
A.滤纸和滤纸装置;B.呼吸模拟器;C.雾化装置
测定法 连接呼吸模拟器(B)和滤纸(置于滤纸装置中)(A)。按药品说明书,取一定体积的药品置于雾化器(C)中。将雾化器吸嘴与滤纸装置连接,必要时使用吸嘴适配器保证气密性。为保证雾化器的放置方向与实际使用方向一致,可适当倾斜呼吸模拟器和滤纸装置。将呼吸模拟器设定为所需呼吸模式。
开启呼吸模拟器,将雾化器的工作时间设定为60s±1s,在呼吸循环的起始时启动雾化器。雾化器的工作时间应能保证定量分析所需的活性物质的量。若60s内滤纸上沉积的活性物质不能满足定量分析要求,可延长雾化器的工作时间;若滤纸饱和,则可缩短雾化器的工作时间。雾化结束后,关闭雾化器。
在过滤装置中放置一张新的滤纸,继续雾化直至雾化完毕。为防止滤纸饱和,必要时可中断雾化更换滤纸。
结果判定 采用各品种项下规定的分析方法,测定各时间段内滤纸和滤纸装置中收集的活性物质量。第一张滤纸收集的活性物质的量与收集时间相比,即为递送速率,所有滤纸和滤纸装置收集的活性物质量的总和,即为递送总量。
【微细粒子剂量】照吸入制剂微细粒子空气动力学特性测定法(通则0951)检查,照各品种项下规定的装置与方法,依法测定,计算微细粒子剂量,应符合规定。
【无菌】除另有规定外,吸入液体制剂照无菌检查法(通则1101)检查,应符合规定。
4.可转变成蒸气的制剂
可转变成蒸气的制剂系指可转变成蒸气的溶液、混悬液或固体制剂。通常将其加入到热水中,产生供吸入用的蒸气。
【微生物限度】除另有规定外,照非无菌产品微生物限度检查:微生物计数法(通则1105)和控制菌检查(通则1106)及非无菌药品微生物限度标准(通则1107)检查,应符合规定。
附表1 吸入粉雾剂递送剂量均一性测定装置的各组成部件
--------------------------------------------------------------------
代码 项目 说明
--------------------------------------------------------------------
A 样品收集管 定量收集递送剂量。与图1描述装置类似,尺寸为
34.85mm(内径)×12cm(长)
--------------------------------------------------------------------
B 滤纸 47mm玻璃纤维滤纸
--------------------------------------------------------------------
C 连接器 内径≥8mm,与P3配套连接的含小直径分支的短金属
--------------------------------------------------------------------
D 真空管 内径≥8mm,内部容积为25ml±5ml合适长度的管道
--------------------------------------------------------------------
E 双向磁通阀 孔口内径≥8mm,开启时间≤l00ms,具有最小气流
阻力的双向双口磁通阀
--------------------------------------------------------------------
F 真空泵 泵需能够以规定流速从整套测定装置和待测吸入剂
抽气。为降低泵容量的要求,使用短和/或宽
(内径≥10mm)真空管连接器将泵与双向电磁阀相连
--------------------------------------------------------------------
G 计时器 计时器需能够按照设定时间驱动双向磁通阀
--------------------------------------------------------------------
P1 压力开关 内径为2.2mm,外径为3.1mm。需与收集管内表面平齐,
位于中心位置,边界清楚,距入口59mm。压力开关P1
不能与大气相通
--------------------------------------------------------------------
P2
P3 压力测量值 绝对压力(P2和P3)
--------------------------------------------------------------------
H 流量控制阀 可调节流量的控制阀,最大额定流量系数(Cν)≥1
--------------------------------------------------------------------
附表2 呼吸模拟器不同呼吸特性
----------------------------------------------------------
项目 特 性
---------------------------------------------------
成人 初生婴儿 婴儿 儿童
----------------------------------------------------------
潮气量 500ml 25ml 50ml 155ml
----------------------------------------------------------
呼吸频率 15循环/min 40循环/min 30循环/min 25循环/min
----------------------------------------------------------
呼吸波形 正弦型 正弦型 正弦型 正弦型
----------------------------------------------------------
吸呼比 1:1 1:3 1:3 1:2
----------------------------------------------------------
① 注:本通则仅作为吸入制剂(吸入气雾剂、吸入粉雾剂、供雾化用的液体制剂可转变成蒸汽的制剂等)生产和质量控制的通用性要求,不作为单独剂型。
数据录入:ningjiajia 校对审核:chujun
(c)药标网 - 中国药典、兽药典质量标准在线查询(豫ICP备16032441号-1)